钒合金具有优良的高温力学性能和低活化特性,是聚变堆中候选的结构材料[1,2]。在结构材料表面制备阻氚涂层是实现大幅降低氚通过渗透进入或渗出结构部件、维持聚变堆氚燃料自持循环、降低氚对材料损伤及人员与环境的放射性危害等诸多不利因素的重要有效途径之一[3,4]。由富Al合金层作为过渡层、Al2O3膜作为外层而组成的铝化物阻氚涂层是中国、欧盟和印度公认的较优阻氚涂层之一[4,5,6],其中Al2O3膜是决定铝化物阻氚涂层最终服役性能的关键所在[4]。目前研究较多的是在铁基合金(如RAFM钢[7,8]、不锈钢[9,10]等)表面制备铝化物阻氚涂层,而关于在钒合金表面制备铝化物阻氚涂层的研究较少。彭雪星[11]通过离子液体镀铝+热处理+氧化处理在钒合金表面成功制备铝化物阻氚涂层,经测试,500 ℃时涂层的阻氘因子为665,但于同样技术下在HR-2钢表面制备的涂层600 ℃时阻氘因子可达1600[10],尚存在不小差距。因此,如何通过选择性氧化处理在V-Al合金层表面形成致密的Al2O3膜成为其应用的关键。然而V-Al合金的氧化机制尚不明确,需对V-Al合金氧化行为、氧化机制及影响因素进行系统研究,从而为获得高性能的铝化物阻氚涂层提供理论指导。
从热力学上看,由于生成氧化物V2O5和Al2O3的自由能相近[15],V-Al合金氧化时会形成V2O5和Al2O3的混合物,而是否形成致密的Al2O3保护膜或者快速生长层则主要取决于金属和金属氧化物的活性,同时也会受氧分压和合金化元素的影响[16,17]。其中,氧化的初始阶段是氧化过程的关键阶段,从理论上讲,理解氧化的微观机制对控制初始阶段的氧化有着非常重要的意义[18,19]。第一性原理计算不仅能够提供丰富的原子尺度信息,而且可以解释很多实验结果,是研究氧化机制的有利手段。Liu等[20,21]和Wang等[22]采用第一性原理方法研究了铌合金和TiAl金属间化合物表面的氧吸附,并构建表面氧化相图,预测了合金发生选择性氧化的可能性。Gong等[23]和Zhang等[24]采用第一性原理研究了金属V中间隙O原子的占位和扩散等行为,在一定程度上解释了金属V的氧化行为,但对于V的氧化机制以及合金元素的作用仍不清楚。
本工作采用第一性原理方法研究了钒合金的氧化机制,包括Al、Ti、Cr等合金元素在V(110)表面的偏析行为,V(110)表面及V(110)-X表面(X=Al、Ti、Cr)的氧吸附行为等。并结合热力学原理构建了表面氧化相图,分析V-Al合金发生选择性氧化的可能性及合金元素Ti和Cr的影响。研究结果对理解钒合金氧化的微观机制、控制氧化的初始阶段具有重要意义。
1 计算模型及方法
对于bcc-V晶胞,k点选择为12×12×12,计算得到的晶格常数为2.997 Å,与其它理论计算值(2.98 Å[23]和2.977 Å[29])和实验值(3.03 Å[30])相一致。对于表面计算,切割优化后的bcc-V晶胞,构建出由7原子层(2×2)-V(110)表面和15 Å真空层组成的板式模型来模拟表面。其中最底3层固定,其余4层原子和吸附的O原子在结构优化中充分弛豫。进行表面计算时,k点选择为9×9×1。表面模型中每层有4个金属原子,单个O原子在(2×2)表面有4种高对称吸附位,分别为顶位(ot)、短桥位(sb)、长桥位(lb)和洞位(3f),如图1所示。表面吸附4个O原子时,O原子的覆盖度Θ=1 ML,合金元素取代表面第一层V原子构成V(110)-X表面。
图1
图1
O原子在V(110)表面吸附位置的示意图
Fig.1
Schematic of possible adsorption sites on the V(110) surface (ot: on-top; sb: short-bridge; lb: long-bridge; 3f: 3-fold hollow)
Color online
式中,
式中,
对于纯净(2×2)-V(110)表面,其表面能(
式中,
对于O/V(110)-X表面体系,其表面能
式中,
利用
本工作研究表面的氧吸附行为,不涉及氧化物的形成,故表面体系中X和O的原子数是独立变化的,则
则
另外,O的化学势(
式中,
2 结果与讨论
2.1 V(110)表面O吸附的稳定性
图2
图2
O原子在V(110)表面不同位置吸附的结合能
Fig.2
Binding energies of oxygen on V(110) surface at different adsorption sites
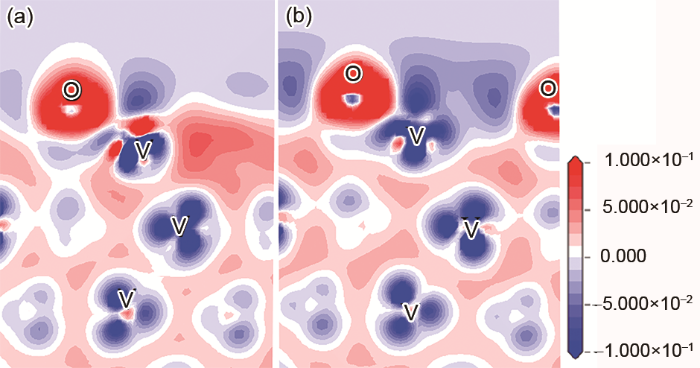
为了深入理解O在V(110)表面化学吸附的本质,分析了O在V(110)表面3f位吸附的差分电荷密度。图3所示为氧覆盖度Θ=0.25和1 ML的差分电荷密度。图中蓝色和红色区域分别代表电荷的失去和得到。可以看出,电荷的重新分布主要发生在吸附O原子和表层V原子之间。电子由表层V原子转移向O原子,导致表面金属电子态的减少。随O覆盖度的增加,表层V原子和吸附O原子之间的电荷转移加剧,表明V—O键的离子性随覆盖度的增加而增强。另外,从图中也可以看出,O原子的吸附只对V(110)的表层原子有影响,次表层以下原子的电荷密度几乎不受O吸附的影响。
图3
图3
覆盖度为0.25和1 ML时O在V(110)面3f吸附位的差分电荷密度图
Fig.3
Charge density difference contours for O adsorbed on V(110) in 3f sites with the oxygen coverage Θ=0.25 ML (a) and Θ=1 ML (b) (The contour plane is along the [
Color online
图4所示为Θ=0.25 ML和Θ=1 ML时,表面吸附O原子和最外层V原子的分波态密度(PDOS)图。覆盖度较低时(Θ=0.25 ML),O的2p电子主要与V的3d电子在-6.25~-4.25 eV能量区间内产生杂化,并与V的3p和4s电子有微弱的相互作用。随O覆盖度增加,O吸附原子与表层V原子的电子相互作用增强。Θ=1 ML时,杂化峰主要位于-7~-3.25 eV能量区间,杂化峰变宽使得O原子与V原子的相互吸引更强。同时-6~-4 eV能量区间有多个峰,推断是O原子之间的杂化,与覆盖度增加导致O原子之间静电斥力增加的分析相对应。
图4
图4
0.25和1 ML覆盖度下O吸附在3f位时O和表层V原子的分波态密度
Fig.4
Partial densities of states (PDOSs) for O and surface-layer V atoms with Θ=0.25 ML (a) and Θ=1 ML (b) when O adsorbed in 3f sites (EF—Fermi level)
2.2 合金化V(110)-X表面
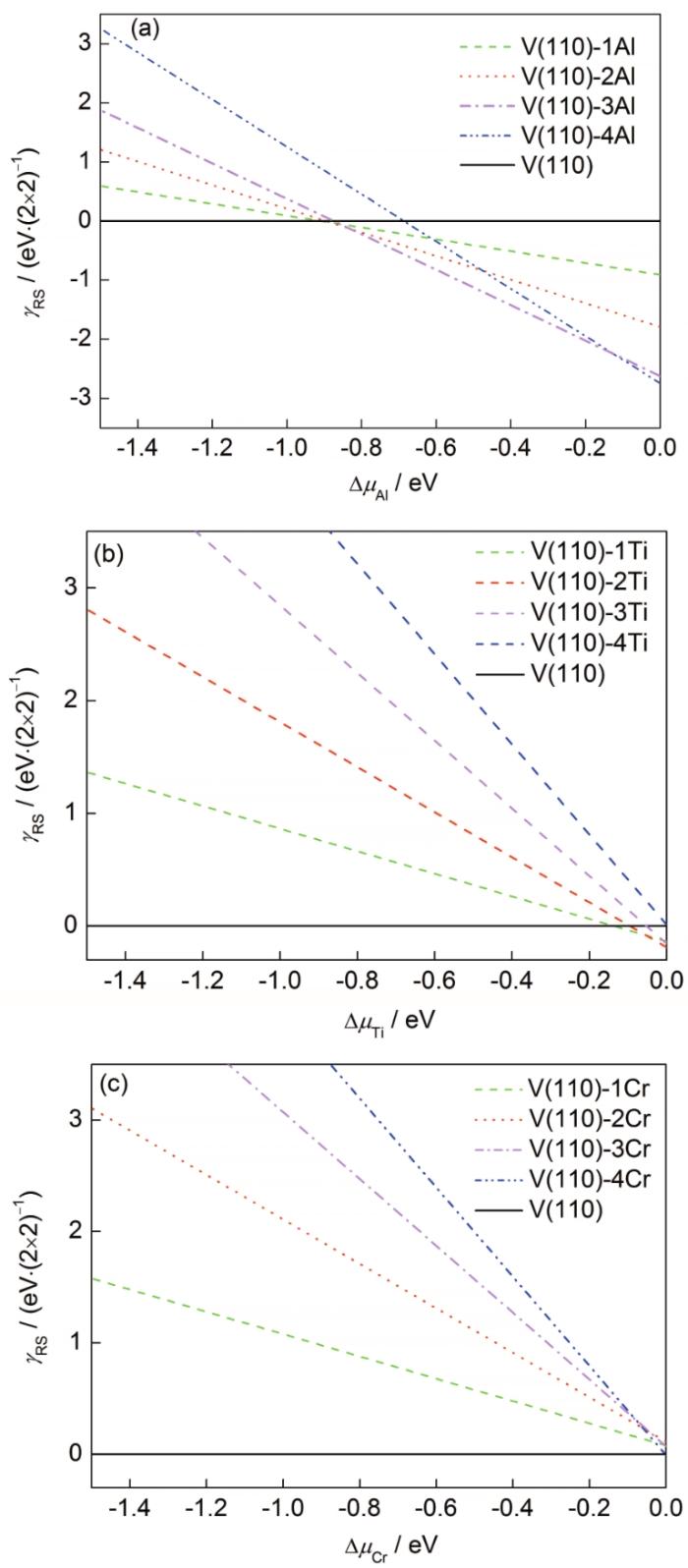
为了研究合金化元素对V(110)表面O吸附行为的影响,首先考察了合金化V(110)-X表面的性质。V(110)-X表面的相对表面能计算结果如图5所示。从表面能上来看,与纯净V(110)表面相比,在富Al(Al化学势较高)的情况下,Al偏析表面更加稳定,V(110)-4Al最稳定。富Ti情况下,Ti偏析表面较纯净V(110)表面稳定,但V(110)-4Ti是个例外,其表面能稍大于V(110)的表面能。富Cr时,V(110)-4Cr的表面能稍低于V(110)的表面能,除此之外,Cr偏析表面均不如纯净V(110)表面稳定。从表面能的结果来看,Al和Ti均有在V(110)表面偏析的倾向,Cr则没有这种倾向。
图5
图5
清洁合金化表面的表面能随合金元素化学势的变化图
Fig.5
The relative surface energies (
2.3 O在V(110)-X表面的吸附
图6所示为O原子在V(110)-X表面的平均结合能。对于O/V(110)-Al体系,从图6a可以看出,随O覆盖度的增加,O原子在V(110)表面的结合(结合能的绝对值)呈下降趋势,而O在Al(111)表面的结合呈增加趋势。O覆盖度较高的情况下,O在Al(111)表面的结合强于O在V(110)表面的结合。表面Al含量较高时[O/V(110)-3Al和O/V(110)-4Al],O在其表面结合能曲线的趋势与O在Al(111)表面的结合能曲线类似。O与V(110)-4Al的结合在覆盖度为1 ML时强于O与V(110)表面及其它Al偏析V(110)表面的结合,表明高O覆盖度有利于Al在V(110)表面的进一步偏析,从而导致Al的选择性氧化。V-Al合金氧化时会形成Al2O3,从而减缓合金的氧化。因此,在钒合金中添加Al元素可以提高其抗氧化性能,与实验结果相符[14,32]。
图6
图6
O在合金化V(110)-X表面的结合能
Fig.6
Oxygen binding energies on the V(110)-Al (a), V(110)-Ti (b), V(110)-Cr (c) surfaces as functions of oxygen coverage
类似地,从图6b可以看出,在本工作考虑的覆盖度范围内,O与Ti(0001)表面的结合强于O与V(110)表面的结合。且随着表面Ti含量的增加,O与Ti偏析V(110)表面的结合增强,说明O的吸附有利于Ti的进一步偏析,从而导致Ti的选择性氧化。
从图6c可以看出,O覆盖度为0.25 ML时,O与Cr(110)表面的结合远远高于O与V(110)表面的结合,随O覆盖度的增加,这种差距逐渐减小。对于O/V(110)-Cr体系,随着表面Cr含量的增加,O与V(110)-Cr表面的结合逐渐减弱,且均弱于O与V(110)表面的结合。这表明O的吸附不会造成Cr的偏析,在V(110)-Cr表面不会发生Cr的选择性氧化。
图7
图7
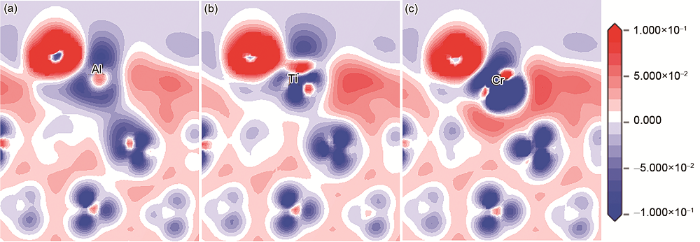
覆盖度为0.25 ML时,O吸附在V(110)-X表面的差分电荷密度图
Fig.7
Charge density difference contours for O adsorbed on V(110)-Al (a), V(110)-Ti (b) and V(110)-Cr (c) with Θ=0.25 ML(Each contour plane is along the [
Color online
图8所示为0.25 ML覆盖度时,V(110)-X表面吸附O原子的分波态密度。与V(110)表面(图4a)相比,表面掺杂Al原子后,Al原子的s和p电子与O原子的p电子分别在-7.75~-6 eV和-6~-4 eV范围内产生杂化,O与表层V原子在-6~-4 eV范围的电子相互作用减弱,在-6.8 eV能量处产生新的杂化峰。表面掺杂Ti原子后,Ti原子的d电子和V原子的d电子均与O原子的p电子在-6.25~-4.25 eV范围内产生相互作用,且Ti原子与O原子的电子相互作用较V原子稍强。表面掺杂Cr原子后,Cr原子的d电子和V原子的d电子与O原子的p电子在-5.5 eV处的杂化峰强度减弱,Cr原子与V原子在-4~0 eV能量范围内的电子相互作用较强。
图8
图8
覆盖度为0.25 ML时O吸附在V(110)-X表面的分波态密度
Fig.8
PDOSs for O adsorbed on V(110)-Al (a), V(110)-Ti (b) and V(110)-Cr (c) surfaces with Θ=0.25 ML
2.4 O/V(110)-X表面体系的热力学稳定性
图9
图9
O/V(110)-Al、O/V(110)-Ti、O/V(110)-Cr的相对表面能及相对表面能相图
Fig.9
The calculated relative surface energies of O/V(110)-Al (a, b), O/V(110)-Ti (c, d) and O/V(110)-Cr (e, f) systems under X rich (a, c, e) and V rich (b, d, f) conditions; and the calculated surface phase diagrams of the relative surface energies for O/V(110)-Al (g), O/V(110)-Ti (h) and O/V(110)-Cr (i) systems (ΔμO—chemical potential of oxygen, p—oxygen partial pressure, p0—standard atmospheric pressure)
Color online
由图9h可知,富O贫Ti时,4O/V(110)更加稳定。富O富Ti时,随Ti的化学势增加,最稳定的表面分别为4O/V(110)-2Ti、4O/V(110)-3Ti、4O/V(110)-4Ti。故V-Ti合金的氧化产物为V和Ti的混合氧化物。
对于O/V(110)-Cr体系,由图9e、f和i可知,不会发生Cr的选择性氧化,故V-Cr合金的氧化产物为V的氧化物。
类似地,对于V-Al-Ti合金的选择性氧化情况,则可以用O/V(110)-Al、O/V(110)-Ti的表面能相图来近似分析。由图9g和h可知,O化学势较高时,根据各元素的化学势,4O/V(110)、4O/V(110)-4Al、4O/V(110)-2Ti、4O/V(110)-3Ti和4O/V(110)-4Ti都能稳定存在。可根据合金的成分以及氧分压等实验条件来分析氧化的过程。如对于V-30Al-10Ti合金,900 ℃在空气中氧化[14],对应富O富V贫Al贫Ti的情况,4O/V(110)的表面能最低,这说明在氧化的最初阶段发生V的氧化。随着氧化的进行,V的化学势降低,Al和Ti的化学势升高,从而发生Al和Ti的氧化。实验发现氧化产物为V2O5、Al2O3和少量TiO2的混合物[14],计算结果可以很好地解释相关的实验现象。
对于V-5Cr-5Ti合金表面制备Al化物阻氚涂层的情况,首先通过离子液体镀Al+热处理,在钒合金表面形成富Al过渡层,然后进行选择性氧化处理在表面形成Al2O3膜[11]。富Al过渡层中Al元素含量最高,其次为V,并含有少量Ti和Cr。对应图9的表面能相图,可以看出,在氧化的最初阶段发生Al的选择性氧化,随着氧化的进行,Al的化学势降低,V和Ti的化学势升高,从而发生V和Ti的氧化。从图9还可以看出,氧分压对于氧化产物的分析影响不大,例如在1200 K温度下,只要氧分压高于10-12 Pa,则各元素氧化的先后顺序和最终氧化产物不会发生变化。但氧化层的生长速度越慢则氧化膜的保护性越好[36],且较低氧分压下V氧化后形成的氧化物为VO2,更有利于形成保护性的Al2O3。因此氧化应在较低的氧分压下进行,以使表面形成连续致密的Al2O3膜。
3 结论
(1) 采用第一性原理方法研究了V(110)表面的O吸附行为以及Al、Ti、Cr等合金元素的影响。结果表明,V(110)表面3f位是稳定的O原子吸附位,随O覆盖度的增加,吸附O原子的稳定性降低。
(2) 表面能的分析表明,Al原子和Ti原子倾向于在V(110)表面偏析,Cr原子不会在V(110)表面偏析。
(3) 结合能的分析表明,O覆盖度较高时Al进一步向V(110)表面偏析,从而造成Al的选择性氧化;类似地,O的吸附有利于Ti的表面偏析,造成Ti的选择性氧化;O的吸附不会引起Cr元素在表面偏析,故不会发生Cr的选择性氧化。因而实验上V-30Al合金氧化产物为V2O5和Al2O3的混合氧化物;V-30Al-10Ti合金氧化产物为V2O5、Al2O3和少量TiO2的混合物,计算结果可以很好地解释相关的实验现象。
(4) 构建了二元钒合金的表面氧化相图,分析了钒合金的选择性氧化行为,与结合能的分析相一致。根据计算结果可以预测V-Al基合金的选择性氧化行为。
参考文献
Present status of vanadium alloys for fusion applications
[J].
Hydrogen transport properties of several vanadium-based binary alloys
[J].
Review on preparation techniques of FeAl/Al2O3 composite tritium permeation barriers
[J].
FeAl/Al2O3复合阻氚涂层制备技术的研究进展
[J].
Tritium permeation barrier-aluminized coating prepared by Al-plating and subsequent oxidation process
[J].
Features of intermetallic compounds in aluminized steels formed using aluminum foil
[J].
An overview on tritium permeation barrier development for WCLL blanket concept
[J].
Comparison of coating processes in the development of aluminum-based barriers for blanket applications
[J].Coming from scales produced by hot dipping aluminization (HDA), the development of processes based on electrochemical methods to produce defined aluminum-based scales on RAFM steels gained attention in research during the last years. Two different electrochemical processes are proposed: The first one, referred to as ECA process, is based on the electrodeposition of aluminum from volatile, metal-organic electrolytes. The other process called ECX is based on ionic liquids.All three processes exhibit specific characteristics, for example in the field of processability, control of coating thicknesses (low activation criteria) and heat treatment behavior. The aim of this article is to compare these different coating processes critically, whereby the focus is on the comparison of ECA and ECX processes. New results for ECX-process will be presented and occurring development needs for the future will be discussed. (C) 2014 Elsevier B.V.]]>
Influence of silicon on hot-dip aluminizing process and subsequent oxidation for preparing hydrogen/tritium permeation barrier
[J].
Study of an iron-aluminide and alumina tritium barrier coating
[J].
A new preparing method and performances of FeAl/Al2O3 tritium permeation barrier
[J].
FeAl/Al2O3阻氚层的制备新方法与性能
[J].
Fabrication and characterization of V-Al/Al2O3 tritium permeation barrier on V-5Cr-5Ti alloy substrate
[D].
V-5Cr-5Ti表面V-Al/Al2O3阻氚涂层的制备及性能研究
[D].
Theoretical analysis of the diffusion processes determining the oxidation rate of alloys
[J].
An extension of Wagner's analysis of competing scale formation
[J].
The high-temperature oxidation behavior of vanadium-aluminum alloys
[J].
Oxidation behaviour of FeAl intermetallics. The effects of Y and/or Zr on isothermal oxidation kinetics
[J].
Effect of Zr additions on the oxidation kinetics of FeCrAlY alloys in low and high pO2 gases
[J].
The initial stages of oxidation of γ-TiAl: An X-ray photoelectron study
[J].
Initial stages of oxidation of Ti45Al7Nb0.4Y alloy at 900 ℃ in air
[J].
Ab initio atomistic thermodynamics study on the oxidation mechanism of binary and ternary alloy surfaces
[J].
Ab initio study of surface self-segregation effect on the adsorption of oxygen on the γ-TiAl (111) surface
[J].
Oxygen adsorption on γ-TiAl surfaces and the related surface phase diagrams: A density-functional theory study
[J].
The stability and diffusion properties of foreign impurity atoms on the surface and in the bulk of vanadium: A first-principles study
[J].
Investigation of the interstitial oxygen behaviors in vanadium alloy: A first-principles study
[J].
Soft self-consistent pseudopotentials in a generalized eigenvalue formalism
[J].
Accurate and simple analytic representation of the electron-gas correlation energy
[J].
Special points for Brillouin-zone integrations
[J].
General methods for geometry and wave function optimization
[J].
Nitrogen adsorption, dissociation, and subsurface diffusion on the vanadium (110) surface: A DFT study for the nitrogen-selective catalytic membrane application
[J].
Incipient FeO(111) monolayer formation during O-adsorption on Fe(110) surface
[J].
Effects of doping elements on oxidation properties of V-Cr-Ti type alloys in several environments
[J].
Influence of Cr, Ti concentrations on oxidation and corrosion resistance of V-Cr-Ti type alloys
[J].
Oxidation performance of V-Cr-Ti alloys
[J].
Effect of oxygen and oxidation on tensile properties of V-5Cr-5Ti alloy
[J].
XPS study of the initial stages of oxidation of α2-Ti3Al and γ-TiAl intermetallic alloys
[J].AbstractThe initial stages of oxidation of α2-Ti3Al and γ-TiAl alloys at 650 °C under low oxygen pressure are shown to be characterized by three stages using XPS. Stage I is a pre-oxidation stage characterized by the adsorption and absorption of oxygen species. When the subsurface is saturated with dissolved oxygen (16 and 2 at.% on α2-Ti3Al and γ-TiAl, respectively), the selective oxidation of the alloy leads to the nucleation and growth of ultrathin (∼0.5 and ∼1.2 nm on α2-Ti3Al and γ-TiAl, respectively) alumina layers (stage II). The growth kinetics of the alumina layers is limited by the transport of Al in the alloy, leading to Al-depletion in the metallic phase underneath the oxide. When a critical concentration is reached (Ti82Al18 and Ti75Al25 on α2-Ti3Al and γ-TiAl, respectively), titanium oxidation occurs (stage III). Ti(III) and Ti(IV) oxide particles are formed at the surface of the still growing alumina layer.]]>