电沉积Ni-Co涂层具有优异的磁学性能,被广泛应用于磁存储产品中,在这类合金中引入Zn可提高其抗高温氧化和耐腐蚀性能[1,2]。多元合金共沉积时,由于异种金属离子还原电位(
络合剂的加入,有助于改善异种金属离子之间的还原析出电位,提高阴极极化,利于实现多元合金异常共沉积[6~9]。抗坏血酸(ascorbic acid,简称H2Asc)或柠檬酸钠(NaH2Cit)作为常见的络合剂,绿色环保,对Ni2+、Zn2+、Mn2+等+2价金属离子均具有较好的络合作用,通过形成络合离子配位化合物,可循环利用,能增强镀液的稳定性和镀液pH缓冲能力,被广泛用于电沉积领域。齐海东等[10]研究Zn-Ni-Mn合金电沉积时发现:随着NaH2Cit浓度增加,金属离子还原受扩散控制的程度在减弱,成核机理由瞬时成核转变为连续成核。Yu等[11]研究了H2Asc对电沉积 Ni-Fe-W合金微结构的影响,结果表明:当H2Asc浓度为3 g/L时,镀层表面光亮致密,耐腐蚀性能好;随着H2Asc浓度增加,沉积速率降低并产生粗大枝晶。Eliaz等[12]对比研究了络合剂明胶(gelatin)和氨基苯磺酸(SA)对Zn-Ni、Zn-Co、Zn-Ni-Co共沉积行为的影响,发现gelatin的加入对离子析出电位影响不大,而添加SA则有利于Co2+电位正移,协同SA + gelatin组合将Zn-Ni-Co还原析出电位正移约200 mV,有助于三元合金共沉积。Bhat和Shet[13]分析了氨基磺酸作为络合剂对Zn-Ni、Zn-Ni-Co电沉积行为的影响,发现适量的氨基磺酸(1 g/L)有利于镀层中Ni含量增大,而≥ 13%的Ni含量则有利于镀层的微结构致密和表面光泽。由上可知,适量的络合剂有助于多元合金异常共沉积,亦可改善其晶体生长结构和耐腐蚀等性能。
鉴于此,本工作以H2Asc作为络合剂,实现Ni-Co-Zn三元合金共沉积。采用CV曲线法优化出适宜的H2Asc浓度,探讨其对电沉积过程中Ni-Co-Zn织构生长的影响;在3.5%NaCl (质量分数)介质中进行电化学测试,揭示γ-Ni5Zn21金属间化合物相及[Zn(OH)4]2-胶质微溶产物所产生的抗腐蚀机制。
1 实验方法
1.1 镀液组分及工艺
经抛光后的紫铜片作为阴极,高纯度石墨为阳极,电极间距为2 cm,电沉积采用SMC-30S型数控双脉冲电源,电流密度3.0~5.0 A/dm2,脉冲频率1.5 kHz,占空比3∶1,脉冲电流换向周期10 ms。基于文献[13]结论并结合Nernst方程,遴选4种离子摩尔浓度比,即Ni2+∶Co2+∶Zn2+ 为1∶1∶1、2∶6∶1、4∶1∶2和4∶5∶1,研究Zn2+浓度对Ni-Co合金组分与结构的影响。
经对比,当Ni2+∶Co2+∶Zn2+摩尔浓度比为4∶5∶1时具有最佳的电化学稳定性,对应的Ni-Co-Zn镀液组分为:0.2 mol/L Ni(SO3NH2)2·4H2O,0.25 mol/L CoSO4·7H2O,0.05 mol/L ZnSO4·7H2O,0.29 mol/L CH3COOH,0.84 mol/L H3BO3,电镀液组分由分析纯试剂配制。为对比研究,络合剂H2Asc添加量分别为0、3、5和10 g/L。用稀H2SO4或氨水调镀液pH值至5左右,镀液温度设定在45℃。为降低电流密度分布差异对阴极表面离子沉积的影响,设定阴、阳极的表观面积比为1∶3。采用双脉冲电沉积制备Ni-Co-Zn镀层,温度为45℃,200 r/min机械搅拌。采用称重法,评估出镀层生长速率为15~20 μm/h,较低的生长速率主要归因于异常共沉积和Zn与Ni、Co发生竞争性的晶体生长规律所致[1,12]。
1.2 表征及性能测试
采用CS150H型电化学工作站进行CV曲线测定,扫描速率20 mV/s,采用标准三电极体系:工作电极和对电极均为石墨电极,参比电极为饱和甘汞电极,电解液为合金镀液,实验设计工作电极表观面积为1 cm × 1 cm,对电极的表观面积为1 cm × 1.5 cm。借助CV曲线确定氧化-还原峰的电势,优化出适宜的H2Asc浓度;并分析H2Asc添加量对优化后三元合金沉积行为的影响。
在3.5%NaCl腐蚀介质中进行电化学性能测试,电化学阻抗谱(EIS)测试扰动信号振幅为5 mV,测试频率范围为0.01~100 kHz;极化曲线的扫描速率为5 mV/s,测试范围为-1.2~1.5 V。在室温环境下,采用3.5%NaCl腐蚀介质对镀层表面进行长时间滴定腐蚀测试,持续滴定48 h后观察其表面腐蚀形态。
采用D8 Advance型X射线衍射仪(XRD)分析电沉积工艺对镀层织构生长的影响,CuKα,波长为0.154178 nm,电子加速功率3 kW,管电流200 mA,扫描速率4°/min,步宽0.02°。借助XRD对各镀层试样经3.5%NaCl水溶液静态浸泡7 d后的腐蚀产物进行物相分析。借助EOS R10相机对涂层试样的宏观形貌进行光学(OM)观察。使用配备有X射线能谱仪(EDS)的S-4800型场发射扫描电镜(SEM)观察试样表面形貌,加速电压5~30 kV,最小分辨率0.1 nm。采用EDS对合金镀层的组分测定,取3点不同位置的平均值。
采用薄片阴极弯曲法,通过测试阴极自由端曲翘位移来评价镀层的内应力。阴极薄片的一面电沉积,另外一面绝缘包覆,电沉积过程中产生的内应力会使得阴极一段发生曲翘,基于张开的角度(α)来计算涂层应力,公式如下[14]:
式中,σ为涂层的内应力(MPa),E为基体的弹性模量(Cu,119 GPa),δ为Cu阴极基体厚度(mm),t为涂层的单面厚度(mm),l为涂层的长度(mm),Z为涂层的顶端偏移量(Z = l × sinα,mm)。
2 结果与讨论
2.1 Zn2+ 浓度对共沉积行为的影响
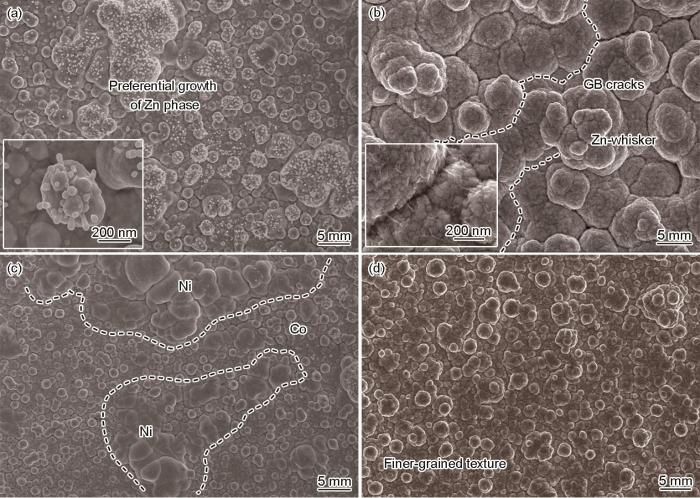
从电化学角度看,Ni2+/Ni和Co2+/Co标准电极电势相近,易实现共沉积;而Zn2+/Zn的标准电极电势较负(-0.76 V),电沉积过程中电势较正的Ni2+或Co2+理应比Zn2+更容易发生还原,然而Zn却比Ni(Co)优先沉积,导致大量的Zn2+被还原析出并吸附在阴极表面,阻碍Ni2+或Co2+放电,致使合金中Ni或Co含量较低。鉴于此,设想通过改变合金镀液中金属离子的浓度来调控镀层中各组元(含量)比例,特别是研究Zn2+浓度对Ni-Co合金组分的影响[15~17]。文献[13]中指出,在硫酸盐体系中,含50 g/L ZnSO4、100 g/L NiSO4、25 g/L CoSO4及少量添加剂等条件下,电沉积Ni-Co-Zn合金结构致密。图1是未添加H2Asc络合剂条件下的三元合金的表面形貌。其中,图1a为Ni2+∶Co2+∶Zn2+ 离子摩尔浓度比为1∶1∶1时,优先放电还原的Zn择优生长,插图显示了类似柱状晶生长结构的Zn晶吸附在活性生长点尖端,阻碍Ni或Co形核生长;随着合金镀液中Co2+ 含量增加(Ni2+∶Co2+∶Zn2+为2∶6∶1),如图1b所示,Zn生长被抑制,形成类似菜花球特征的形貌特征,由于过程中Zn2+与Ni2+或Co2+发生竞争性结晶生长,致使生长应力较大而出现许多晶界(GBs),然而形成的棉絮状Zn晶须犹如柔性绳索作用于GBs来约束并抑制应力开裂(见图1b插图),这主要归因于阴极区域Zn2+扩散受到浓差极化控制,快速消耗的Zn2+得不到及时补充。图1c显示镀液中Ni2+∶Co2+∶Zn2+为4∶1∶2时,晶粒细化且镀层表面致密,部分粗大的织构可能是Ni晶发生自催化形核择优生长所致;鉴于此,进一步优化离子浓度比,在Ni2+∶Co2+∶Zn2+ 为4∶5∶1条件下获得了结构完整性好和晶体均匀细化的三元合金镀层,如图1d所示,说明此条件下Zn2+没有发生瞬间爆发性形核生长,这主要归功于具有自催化活性的细晶Ni来充当晶胚,细化晶粒并抑制了Zn的择优生长。
图1
图1
不同合金离子摩尔比条件下Ni-Co-Zn三元合金表面形貌的SEM像
Fig.1
SEM images showing surface features of deposited Ni-Co-Zn alloys within different ionic molar concentration ratios of Ni2+∶Co2+∶Zn2+ (Insets in Figs.1a and b show the locally high magnified images; GB—grain boundary)
(a) 1 ∶ 1 ∶ 1 (b) 2 ∶ 6 ∶ 1 (c) 4 ∶ 1 ∶ 2 (d) 4 ∶ 5 ∶ 1
表1 离子摩尔浓度比对Ni-Co-Zn合金成分的影响 (atomic fraction / %)
Table 1
| Ni ∶ Co ∶ Zn | Ni | Co | Zn |
|---|---|---|---|
| 1 ∶ 1 ∶ 1 | 3.70 | 2.38 | 93.92 |
| 2 ∶ 6 ∶ 1 | 5.24 | 3.05 | 91.71 |
| 4 ∶ 1 ∶ 2 | 7.13 | 6.81 | 86.06 |
| 4 ∶ 5 ∶ 1 | 12.14 | 20.22 | 67.64 |
2.2 循环伏安曲线
关于Ni-Co-Zn异常共沉积,常用氢氧化物抑制机制来解释[18]。共沉积时,随着阴极表面H2的析出,溶液pH值升高而生成Zn(OH)2膜,抑制了Ni或Co的析出。此外电极表面Zn(OH)2又易于放电还原为Zn,从而发生大量的Zn优先析出。为促使Ni-Co-Zn合金由异常共沉积转变成正常共沉积,添加络合剂组成缓冲溶液到镀液中,以减少阴极表面的pH值变化和氢氧化物的生成。
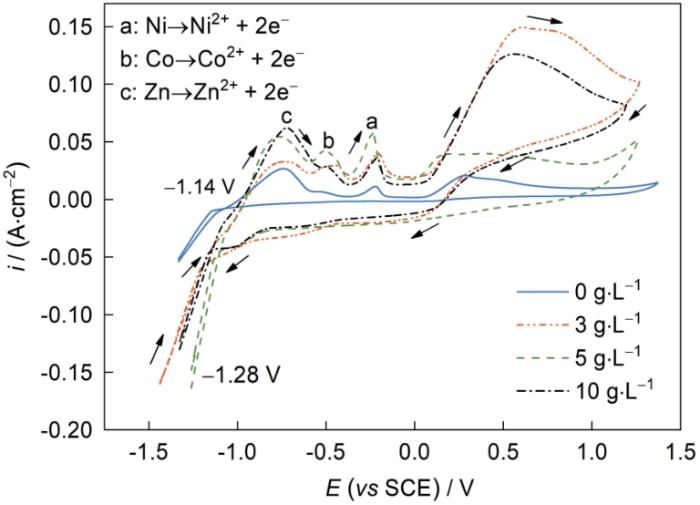
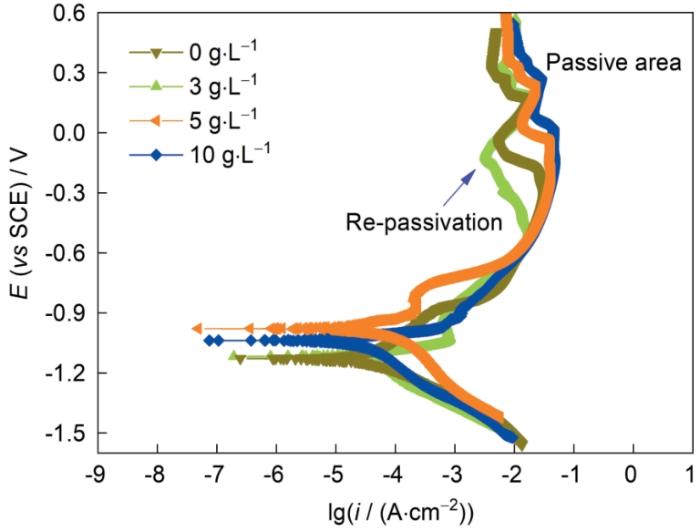
在优化得出最佳的离子摩尔浓度比(Ni2+∶Co2+∶Zn2+ = 4∶5∶1)基础上,进一步研究H2Asc浓度对三元合金异常过程行为的影响。图2所示为不同H2Asc浓度条件下合金镀液的CV曲线,均出现了特征明显的3个氧化峰,位置a、b和c分别对应于Ni、Co和Zn的氧化峰或是金属单质溶解或是Ni5Zn21金属间化合物被溶解,仅存在1个较为明显的还原峰位于-1.28 V附近,对应于3者的合金化合物还原析出峰(如Ni5Zn21、CoZn13等相),没有出现明确的单质还原峰,这与文献[7,13~15]中结论类似,说明三元Ni-Co-Zn的共沉积过程受电化学控制。区别是,添加H2Asc后的合金镀液CV曲线上出现了高而宽的氧化峰,在负向扫描至-1.28 V后电流密度陡然增大,这主要归因于HAsc-和Zn2+形成[ZnHAsc]+配位离子并吸附到电极附近,从而阻碍Ni2+和Co2+放电还原,持续负向扫描,一旦突破电极表面的富Zn相,在-1.5 V附近发生了合金共沉积。实验过程中,当负向扫描至-0.75 V时,工作电极上陆续出现深灰色的金属沉淀物,继续负向扫描则沉淀物增加,从而验证了在-1.28 V附近发生了还原沉积,说明离子摩尔浓度比优化后的合金镀液在HAsc-协同作用下发生了合金共沉积。当H2Asc浓度为5 g/L,CV曲线正向扫描至0.2 V时,没有发生电流密度激增的现象,说明随着电压增加未发生快速氧化,可见镀液稳定性较好;负向扫描至对应拐点的还原峰位置,较未添加H2Asc镀液正移且负向电流密度最大,还原电位正移了约0.36 V,说明发生还原放电较为容易,有利于合金共沉积。随着H2Asc的浓度增加至10 g/L,还原峰负移,共沉积难度增加,这主要归因于过高浓度的H2Asc发生析氢反应,并与Zn形成的配位化合物覆盖到电极表面,阻碍了Ni2+和Co2+离子放电还原。
图2
图2
不同H2Asc浓度条件下Ni-Co-Zn合金镀液的循环伏安曲线
Fig.2
Cyclic voltammogram curves for Ni-Co-Zn deposits from the electrolytic baths within different H2Asc concentrations at a scan rate of 10 mV/s (i—current density, E—potential, SCE—satured calomel electrode)
2.3 H2Asc浓度对合金镀层形貌及成分的影响
相较于传统柠檬酸盐络合剂,H2Asc作为一种绿色环保型络合剂,电沉积过程中能够循环使用,络合活性更强,能通过自身携带的自由基∙H键与+2价金属阳离子(M2+)发生离子交互,过程中作为载体将与M2+形成配位化合物,以缩减异种金属离子的还原电位差来实现合金共沉积[19,20]。关于络合机理,H2Asc与柠檬酸钠(Na3Cit)类似,经多次分解形成HAsc-和Asc2-,有利于缓冲溶液pH值和形成配位化合物作用,对M2+具有很强的络合能力,形成[MHAsc]+型配位化合物。陈与德[21]通过实验得出在同等条件下络合能力强弱次序:Fe2+ < Co2+ (Zn2+) < Ni2+ < Cu2+,其中Zn2+与Co2+的络合能力相当。也就是说,在络合反应过程中HAsc-与Ni2+形成[NiHAsc]+的稳定常数最大,不易被解离,不易被还原。同时,HAsc-与Co2+、Zn2+形成的稳定常数基本相当,小于Ni2+的稳定常数,容易被还原。考虑到实际电沉积过程中Zn2+易发生欠电位式的异常电沉积,所以Ni-Co-Zn合金中Zn含量最大。这与本实验结果基本吻合。
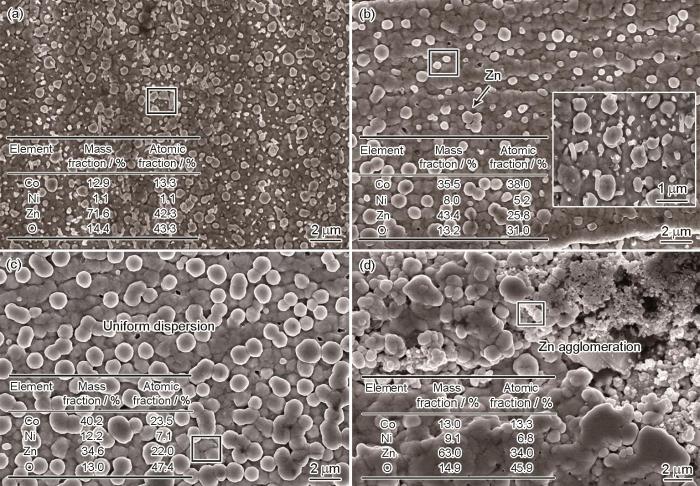
图3为Ni2+∶Co2+∶Zn2+ = 4∶5∶1条件下,不同H2Asc浓度合金镀层表面形貌的SEM像。添加H2Asc前后的形貌特征发生了显著变化。未添加时,如图3a所示,图中白色斑点为ZnO相,共沉积过程中Zn2+发生了优先还原,斑点相ZnO不均匀地结晶析出,Ni和Co被抑制生长,合金共沉积效果不佳。添加3 g/L H2Asc后,如图3b所示,ZnO白色斑点减少,从其插图可以看出少量Zn沿夹缝向外生长,说明H2Asc的加入有效阻止了ZnO相的富集生长,出现了大-小颗粒相互嵌套的织构生长特征。随着H2Asc浓度增加至5 g/L,合金镀层结构致密均匀且晶粒呈现椭圆特征,如图3c所示,部分析出ZnO尺寸为300~500 nm,没有出现明显的ZnO相富集和GBs开裂等缺陷。提高H2Asc浓度至10 g/L时,镀液中大量的HAsc-不仅与Zn2+络合形成[ZnHAsc]+,亦能与Co2+和Ni2+发生作用,使放电离子的平衡电位变负,不利于合金镀液中离子的扩散,使合金原子无法爆发式瞬时成核,导致合金中的Ni + Co总含量下降,出现了晶粒尺寸不均匀和Zn富集的现象,如图3d所示。
图3
图3
不同H2Asc浓度条件下合金镀层表面形貌SEM像和EDS分析
Fig.3
SEM images showing surface features of Ni-Co-Zn deposits within different H2Asc concentrations (Insets show the EDS results of square-located areas and the locally high magnified image)
(a) 0 g/L (b) 3 g/L (c) 5 g/L (d) 10 g/L
为研究H2Asc浓度对合金镀层中组分含量的影响,采用EDS对其成分进行测定,图3中各插图为局部区域EDS测试结果。可见,随着H2Asc浓度由0 g/L增加至5 g/L时,镀层中Zn含量逐渐降低,Ni + Co含量增加,图3c中Ni含量高达12.2%,通常合金镀层中Ni含量≥ 12%时,有利于细晶生长,同时抑制Zn择优生长,结构致密[16,21]。随着H2Asc浓度增加至10 g/L时,镀层中Zn含量高达63.0%,同时Co含量明显减少,Ni含量降低至9.1%,这主要是由于大量的H2Asc在镀液中会失去一个自由基∙H后与被还原的Zn2+形成配位化合物[ZnHAsc]+ 吸附到阴极表面,抑制了Ni2+和Co2+的放电被还原,胶体理论可以解释这种异常共沉积现象。此外,所有试样中的O含量较高,可能是由于表面活性元素Zn被氧化成ZnO所致。
2.4 XRD物相分析
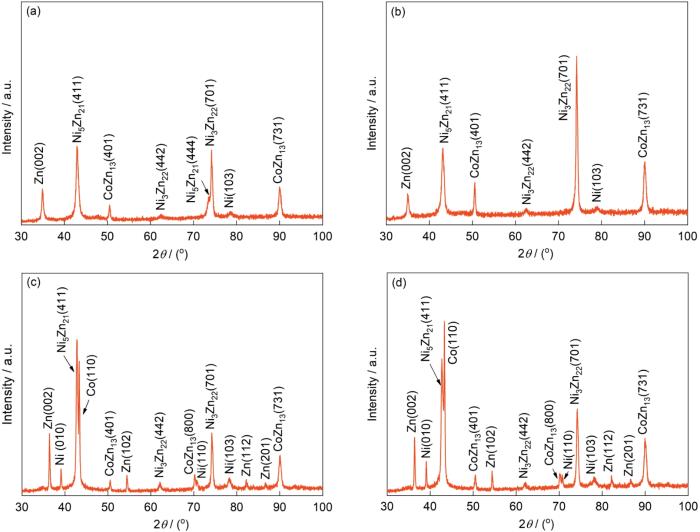
图4为不同H2Asc浓度条件下Ni-Co-Zn镀层试样的XRD谱。未添加H2Asc时,如图4a所示,在35.1°附近出现了Zn(002)和78.7°的Ni(103)衍射峰,其余则为Ni5Zn21、CoZn13和Ni3Zn22等化合物相。随着H2Asc浓度从3 g/L提高至5 g/L,再增加至10 g/L,如图4b~d所示,总体上,3种条件下镀层试样的织构呈多方向生长,相组分不单一,不仅存在单质相,还存在明显的化合物相如Ni5Zn21(411)、CoZn13(401)、CoZn13(731)、Ni3Zn22(442)、Ni3Zn22(701),实现了合金化共沉积效果。这一结论与上述CV曲线中仅出现一条还原峰结论吻合,即以金属间化合物还原析出为主。此外,在5 g/L浓度条件下(图4c),在39.1°和78.7°分别增加了单质相Ni(010)和Ni(103),在43.2°附近出现了金属单质Co(110)。较多金属单质的出现,特别是具有自催化形核作用的Ni析出,充当后续异质形核位点,有利于细晶强化;金属间化合物γ-Ni5Zn21相(PDF# 06-0653)的出现有利于镀层强韧性,特别是耐腐蚀性能。综上所述,适量H2Asc络合剂作用下,Zn2+与Ni2+、Co2+能发生还原共沉积,但Ni-Zn合金相析出较Ni-Co相活跃,这主要归因于2方面:(1) 三元沉积过程中,无论H2Asc量的多少,Zn2+放电还原始终占主导地位,优化析出的Zn吸附到Ni或Co活性尖端抑制其生长,最终出现少量Ni或Co从ZnO缝隙生长;(2) 被还原析出的纳米晶Ni具有自催化作用,形成晶胚与Zn产生竞争生长,从而抑制Zn的择优生长,细化晶粒[22]。
图4
图4
不同H2Asc浓度对电沉积Ni-Co-Zn合金织构生长影响的XRD谱
Fig.4
XRD spectra showing textural evolution for Ni-Co-Zn deposits within different H2Asc concentrations
(a) 0 g/L (b) 3 g/L (c) 5 g/L (d) 10 g/L
2.5 生长应力分析
电沉积Ni-Co-Zn属于一种典型的异种共沉积行为,过程中Zn2+优先放电还原并以
图5
图5
不同H2Asc浓度对生长应力影响的镀层表面OM像
Fig.5
OM images showing surface deformations by growth stresses for the as-deposited samples with different H2Asc concentrations (Z—initial length of Cu substrate for deposit, l—length of deposit, α—the angle at which the cathode is warped, σ—interior stress of deposit)
(a) 0 g/L (b) 3 g/L (c) 5 g/L (d) 10 g/L
采用薄片阴极弯曲法对各镀层试样的内应力进行测试,测试结果列于图5各图右上角。可见:当H2Asc浓度为5 g/L时,镀层表现出的张应力最小,为9.04 MPa,这主要归因于适量的H2Asc抑制了Zn的择优取向,调控了三元合金中各相比例,其中降低Zn含量有助于细化晶粒,减少了由于Zn团聚或晶格畸变而引起的生长应力。
H2Asc作为一种高效络合剂,经水解后与Zn2+形成[ZnHAsc]+配位化合物,可抑制Zn择优生长,减少Zn(OH)2沉淀膜的生成,以促进Ni-Co-Zn三元合金共生长。为观察H2Asc浓度对织构生长应力的影响,采用FE-SEM对其微观形貌进行表征。未添加H2Asc时,如图6a所示,出现许多微裂纹和白斑(ZnO相),由于过量的Zn择优生长并粗化,半导体ZnO相的物化性质与Ni或Co存在很大差异,导致织构生长兼容性差,镀层出现微裂纹开裂。Kurachi和Fujiwara[24]研究得到类似结果,镀液中Zn2+浓度过高,导致镀层中Zn/Ni组元含量比例失衡,过量的Zn易引起高的内应力。图6b为添加3 g/L H2Asc后的合金镀层,存在少许微裂纹,ZnO相夹着缝隙生长,氧化形成的ZnO枝晶会穿孔而出,从而诱发镀层表面开裂。添加5 g/L后,从图6c观察可知,镀层表现发生了明显变化,平整且致密度高,仅有少许粗晶Ni析出,这与图5c中的弯曲幅度是吻合的。当H2Asc浓度进一步增大至10 g/L时,如图6d所示,镀层表面粗糙且存留一些轻微的裂纹,凹凸不平的表面夹杂一些轻微裂纹,这主要是由于过量的H2Asc经水解形成大量的∙H自由基并吸附到阴极表面,原子状态的H或者H2分子在电沉积过程中扩散到镀层金属晶格缺陷处,析氢产生的气泡外溢,造成镀层收缩,从而导致形成较多长条状的小裂纹。
图6
图6
不同H2Asc浓度条件下镀层试样表面的SEM像和EDS分析
Fig.6
SEM images showing surface features for tested samples with different H2Asc concentrations (Insets show the EDS results for the square-located areas in Figs.6b and c)
(a) 0 g/L (b) 3g/L (c) 5g/L (d) 10g/L
2.6 耐腐蚀性能
2.6.1 动电位Tafel曲线
式中,ΔE为外加极化电位(mV);ΔI对应于极化电位下的电流密度(A/cm2);ba和bc分别对应于极化曲线中阳、阴极化曲线的斜率,测试结果列于表2。可以看出,较未添加H2Asc的试样,含5 g/L镀层的icorr降低了约75%,耐腐蚀性能显著增强;自腐蚀电位(Ecorr)也正移了约150 mV,大大降低了自腐蚀反应的驱动力,这主要归功于ZnO相弥散析出至微孔和缺陷区域,提高了镀层的致密度;同时,随着H2Asc的介入,Zn2+还原被抑制并被后续Ni自催化形核取代,细化组织,同时形成的Ni5Zn21等合金化合物沿着应力开裂的GBs弥散析出,提高了镀层的致密度[26,27]。在中性NaCl腐蚀介质中,少量游离态的Zn2+与吸氧产物OH-形成
图7
图7
不同H2Asc浓度条件下合金镀层试样的动电位极化曲线
Fig.7
Potentiodynamic polarization curves of tested samples immersed in 3.5%NaCl solution
表2 由极化曲线得到的各镀层相关电化学参数
Table 2
c g·L-1 | bc mV·dec-1 | ba mV·dec-1 | Ecorr mV | icorr 10-6 A·cm-2 | Rp kΩ |
|---|---|---|---|---|---|
| 0 | 149.14 | 158.79 | -1127.9 | 1.58 | 21.10 |
| 3 | 148.33 | 161.15 | -1117.5 | 0.75 | 44.69 |
| 5 | 159.32 | 174.13 | -979.2 | 0.40 | 83.10 |
| 10 | 121.47 | 64.98 | -1038.7 | 0.43 | 45.84 |
2.6.2 EIS分析
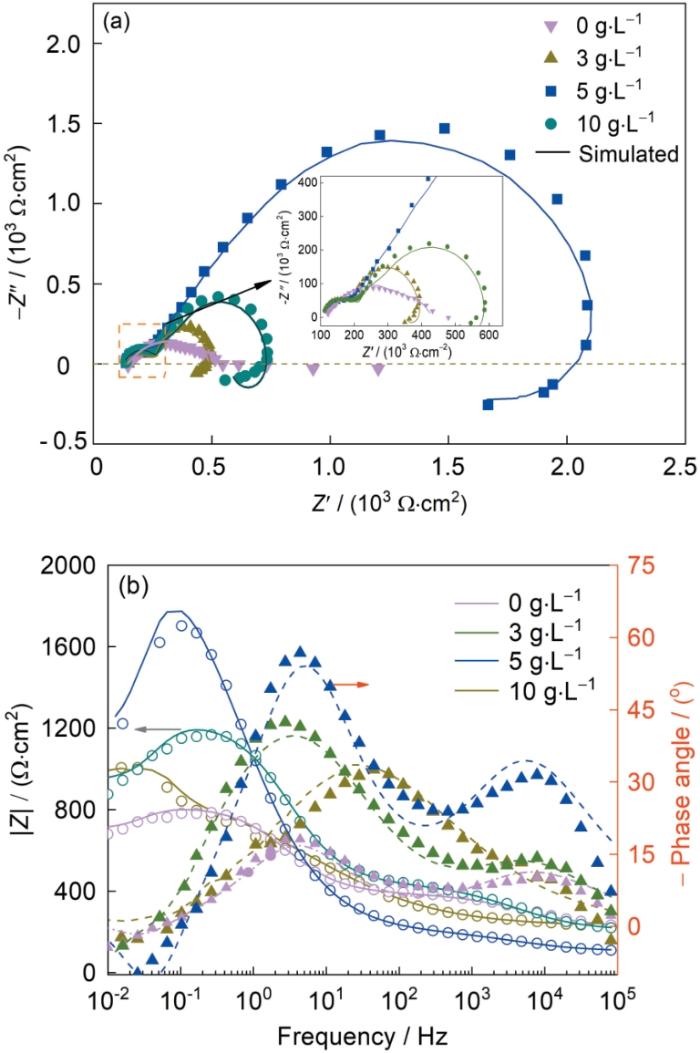
EIS是一种基于准稳态条件下研究电极表面特性的技术,该技术只需要对于准稳态体系施加一个很小的正弦波扰动,对于电极表面影响较小。图8a为Nyquist图。可知:不同H2Asc浓度条件下的试样具有类似的Nyquist图,均由一个高频容抗弧和中低频感抗弧组成,其中含5 g/L H2Asc试样的感抗弧半径最大,半径越大表示阳极析氧反应时转移电荷所受到的阻值越高,抗腐蚀性能越好。未添加H2Asc的试样,由一个高频容抗弧和中低频扩散弧组成,其镀层试样表面存在的活性Zn相会发生溶解,易诱发点腐蚀并在中低频区出现了Warburg扩散阻抗;添加H2Asc后的合金试样中,Zn含量降低,较多的单质Ni和Co还原析出,形成的Ni5Zn21等化合物弥散析出并封堵了点蚀源,减少Cl-扩散渗透的渠道。
图8
图8
不同H2Asc浓度条件下电沉积的合金镀层试样的电化学阻抗谱(EIS)
Fig.8
Electrochemical impedance spectroscopy (EIS) of tested samples with different H2Asc concen-trations immersed in 3.5%NaCl solution (Z'—real part of AC impedance, Z''—imaginary part of AC impedance, |Z|—the total impedance)
(a) Nyquist plots (b) Bode plots
图8b为Bode图。从频率(f)与相位角之间的变化规律可知,2个波峰对应于2个时间常数,分别为镀层试样在腐蚀溶液中的电化学溶解和活性Zn经水解后形成的微溶腐蚀产物覆盖至被刻蚀的活性表面,其中:添加3和5 g/L H2Asc后,试样的Bode图中的波峰具有最大的相位角,在中频区(103~100 Hz),lgf与阻抗(|Z|)之间表现为较明显的线性关系,显示出良好的电容特性,说明镀层表面完整性好;然而,低频区(10-2~100 Hz),特别是添加5 g/L H2Asc后试样的低频区|Z|值较未添加H2Asc试样提高约5倍,在较宽的频率变化范围内保持着最大的相位角(接近60°),在此区域|Z|与lgf之间线性关系的斜率变大,可见腐蚀速率增大,这主要归因于大量活性Zn在含Cl-的腐蚀介质中发生了活化溶解和得失电子(Zn→Zn2+ + 2e-),从而加速了电极表面电荷转移速率。
2.6.3 等效电路及其解析
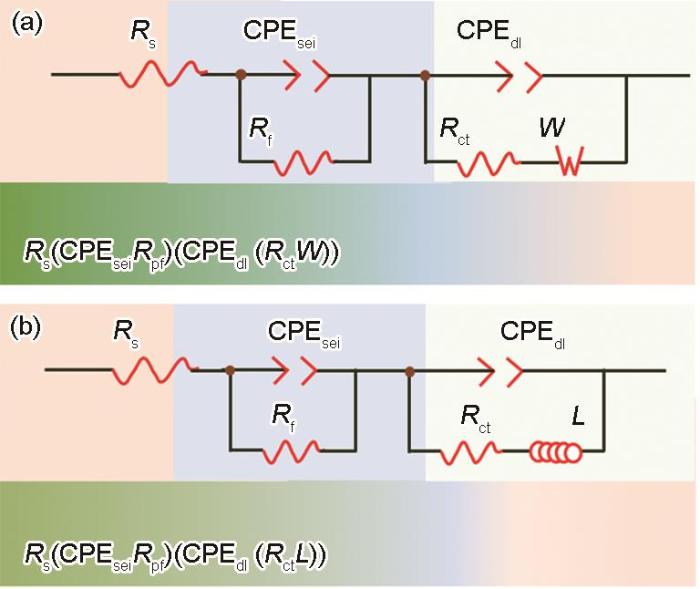
为准确描述Ni-Co-Zn镀层试样在3.5%NaCl腐蚀介质中的电化学腐蚀行为,引入等效电路(EECs)对其腐蚀界面机理进行模拟和分析。据合金镀层的相成分差异,被腐蚀的区域大致分为2部分:一部分是由于裸露的活性Zn发生电化学溶解而裸露出的活性金属表面;另一部分则为被Zn(OH)2或富Zn微溶腐蚀产物所覆盖的腐蚀面。由于具有小离子半径的Cl-沿镀层局部活性点吸附并侵蚀造成孔核,易诱发点蚀,用Warburg元件拟合。在中性NaCl溶液中,阳极发生的是金属溶解并形成离子的过程;阴极反应主要是O2还原并生成OH-,致使阴极区pH值升高,金属阳离子与OH-生成Zn(OH)2等微溶产物覆盖在腐蚀面上,从而引起感抗效应。根据上述EIS特征并结合文献[10,29]中提出的关于Ni-Zn镀层在3.5%NaCl腐蚀介质中的等效电路,未添加和添加不同H2Asc浓度下试样的等效电路分别对应于Rs(CPEseiRpf)(CPEdl(RctW))与Rs(CPEseiRpf)(CPEdl(RctL))模型,采用Zview软件对所测EIS进行EECs拟合与解析,如图9所示,各元件数据拟合结果列于表3。其中:Rs为溶液电阻,Rct为电极(镀层)电荷转移电阻,Rpf为钝化膜的电阻(如Zn(OH)2沉淀膜),W表示溶液中Cl-扩散渗透到腐蚀产物所形成Warburg扩散阻抗,L代表胶质微溶腐蚀产物在蚀孔表面吸附而引起的感抗;CPEdl和CPEsei分别对应于镀层与溶液之间的双电层电容和钝化膜电容。考虑到电极表面弥散效应,理想电容被常相位元件(CPE)代替,其阻抗ZCPE可表示为:
式中,ω为角频率(2πf),rad/s;n和Y0分别对应于双电容弥散系数和相位角常数。
图9
图9
拟合EIS采用的等效电路图
Fig.9
Equivalent circuits fittings for tested samples without (a) and with (b) H2Asc addition (Rs—solution resistance, Rct—charge transfer resistance, Rpf—passive layer resistance, CPEdl—double layer capacitance, CPEsei—passive layer capacitance, L—equivalent inductance, W—Warburg impedance )
表3 基于等效电路的EIS拟合结果
Table 3
c g·L-1 | Rs Ω·cm2 | CPEsei Ω-1·s | nf | Rpf Ω·cm2 | CPEdl Ω-1·s | nd | Rct Ω·cm2 | L H·cm-2 | W Ω·cm2·s0.5 | Error|Z| 10-3 |
|---|---|---|---|---|---|---|---|---|---|---|
| 0 | 11.40 | 5.83 × 10-3 | 0.453 | 32.25 | 2.64 × 10-7 | 0.423 | 7.76 | - | 2.33 × 10-9 | 5.562 |
| 3 | 11.17 | 6.44 × 10-3 | 0.726 | 24.16 | 9.36 × 10-5 | 0.696 | 7.89 | 30.65 | - | 5.375 |
| 5 | 8.77 | 2.05 × 10-3 | 0.729 | 172.1 | 2.46 × 10-3 | 0.370 | 18.62 | 40.71 | - | 3.734 |
| 10 | 11.19 | 7.93 × 10-3 | 0.670 | 32.46 | 7.96 × 10-5 | 0.711 | 7.62 | 4.02 | - | 5.270 |
根据拟合结果的总体误差(Error)分析可知,该电路适用于该体系。
2.6.4 腐蚀产物
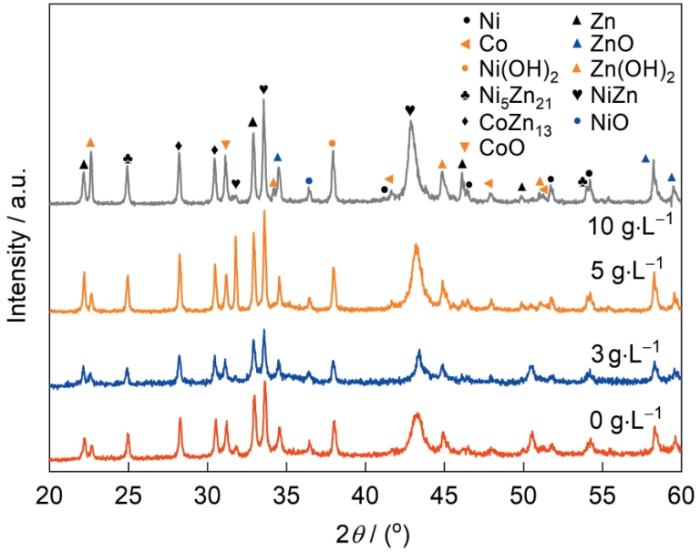
对腐蚀产物的XRD物相分析如图10所示。所有试样的腐蚀产物中均含Zn(OH)2、Co(OH)2、Ni(OH)2等,还出现了Ni5Zn21、CoZn13等化合物。然而,添加不同浓度H2Asc后的试样,在24.8°附近Ni5Zn21相的峰强逐渐变大,同时在51.8°和54.2°出现了较为明显的单质Ni相,进一步说明络合剂H2Asc 的加入有助于抑制Zn生长,除了上述这些主要腐蚀产物外,还出现了NiO和CoO等相,这主要归因于具有抗氧化作用的H2Asc可抑制金属离子被氧化,出现NiO等相可减少Zn(OH)2向疏松多孔的ZnO相转变。经水解反应生成的Zn(OH)2膜比较致密,具有黏附性,能吸附到点蚀坑以抑制腐蚀的进行[30]。Byk等[31]根据Zn-Ni相图认为形成的γ-Ni5Zn21相可减少局部电池,耐腐蚀性能好。此外,微溶相Ni(OH)2、Co(OH)2及Zn(OH)2等产物积累并团絮成胶状物,具有黏附性,填充到“闭塞微孔电池”内部,减少或阻碍活性Cl-向内扩散渗透,能显著提高其耐腐蚀性能。
图10
图10
静态浸泡7 d后试样表面腐蚀产物的XRD谱
Fig.10
XRD spectra of corroded products for samples immersed in 3.5%NaCl solution for 7 d
2.6.5 耐腐蚀机理分析
有关Zn-Ni合金的腐蚀机理研究较为成熟,但Ni-Co-Zn三元合金的研究较少,特别是Co的加入不仅可以调节合金中Zn与Ni含量,还可显著提高Zn-Ni镀层的抗腐蚀性能。通常,Ni含量不同,其晶体结构和腐蚀产物也不同,其耐蚀机理也不一样。已有研究[32,33]表明:镀层中Ni含量为10%~20%时,Ni与Zn或Co形成金属间化合物,为连续的γ-Ni5Zn21或CoZn13相合金,具有好的热力学稳定性,耐腐蚀性能最好;当Ni含量< 5%时,其腐蚀产物主要是结构疏松的ZnO,没有防护性。本工作以3.5%NaCl作为腐蚀介质,探讨了室温环境下添加H2Asc对合金镀层表面耐蚀机理的影响。未添加H2Asc的镀层试样表面布满了被溶解后遗留下的边缘清晰的腐蚀坑,点蚀坑较深。相比之下,添加H2Asc后的试样表面则呈现均匀腐蚀,仅出现了少量不溶解的腐蚀产物,尤其是H2Asc浓度为5 g/L时,镀层表面腐蚀坑轻微且被腐蚀产物覆盖。这主要归功于适量的H2Asc能有效调节合金中的Ni含量,部分Ni氧化成NiO,减缓了腐蚀动力并促使生成的
阳极反应:
阴极反应:
浸泡过程中形成的胶状微溶产物:
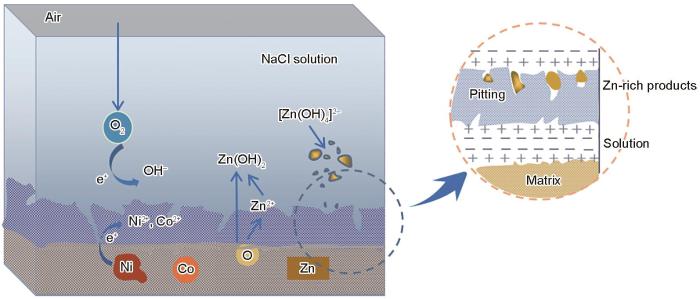
在含Cl-的腐蚀介质中静态浸泡,其腐蚀机理如图11所示。随着浸泡时间延长,Cl-穿透镀层新鲜表面并诱发吸氧腐蚀,pH值升高,促使Zn2+经水解形成
图11
图11
静态浸泡过程中Ni-Co-Zn合金镀层的腐蚀机理示意图
Fig.11
Schematic of corrosion mechanism for Ni-Co-Zn ternary coatings in 3.5%NaCl solution
3 结论
(1) 基于CV曲线,明确了络合剂H2Asc对Ni-Co-Zn异常共沉积行为的影响规律。电沉积过程中,络合剂H2Asc提供配体HAsc-并与Zn2+形成[ZnHAsc]+配位化合物,吸附在阴极表面,提高阴极极化。当H2Asc添加量为5 g/L时,CV曲线上的还原电位峰正移了约200 mV,促进了Zn2+与Ni2+、Co2+共沉积,此时合金中Ni含量高达12.2%,晶粒细化致密。
(2) 当[Ni2+]∶[Co2+]∶[Zn2+]摩尔浓度比为4∶5∶1时,织构生长呈类菜花球状,形成大-小晶粒相嵌共生的特征,晶粒尺寸约300 nm;XRD谱测定出该合金镀层中存在Ni5Zn21、NiZn和CoZn13等金属间化合物相,显示出较好的共沉积效果。
(3) 添加5 g/L H2Asc后的镀层试样具有最佳的耐腐蚀性能,Ecorr正移了约200 mV,icorr为4.0 × 10-7 A/cm2,较未添加的试样降低了约75%,这主要由于适量H2Asc有助于获得高Ni含量(≥ 12%)并同时降低Zn含量,形成了结构致密的复合镀层。在3.5%NaCl腐蚀介质中,镀层中γ-Ni5Zn21相和形成的
参考文献
Influence of Ni2+ concentration and deposition potential on the characterization of thin electrodeposited Zn-Ni-Co coatings
[J].
Surface microstructure and corrosion resistance of electrodeposited ternary Zn-Ni-Co alloy
[J].
Study on electrodeposition preparation and corrosion resistance of Zn-Ni alloy
[J].
电沉积制备Zn-Ni合金及其耐蚀性的研究
[J].
Influence of Ni2+/Co2+ ratio in electrolyte on morphology, structure and magnetic properties of electrolytically produced Ni-Co alloy powders
[J].
Electrochemical deposition and corrosion stability of Zn-Co alloys
[J].
Effects of dispersant on performance of Ni-Zn batteries
[J].
Influence of additives on microstructure, mechanical and tribological properties of nanocrystalline Zn-Ni coatings in a novel alkaline bath
[J].
Wafer level electrodeposion of Fe-Ni novel UBM films
[J].
Fe-Ni新型UBM薄膜的晶圆电镀工艺研究
[J].
Influence of Co2+ ions concentration in a galvanic bath on properties of electrolytic Zn-Ni-Co coatings
[J].
Effect of sodium citrate on Zn-Ni-Mn alloy electrodeposition behavior
[J].
柠檬酸钠对Zn-Ni-Mn合金电沉积行为的影响
[J].
Effect of processing parameters and ascorbic acid on the electrodeposition NiFeW alloy coatings
[J].
Electroplating and characterization of Zn-Ni, Zn-Co and Zn-Ni-Co alloys
[J].
Development and characterization of Zn-Ni, Zn-Co and Zn-Ni-Co coatings
[J].Acidic sulphate baths having ZnSO4 7H(2)O, NiSO4 7H(2)O, CoSO4 7H(2)O and sulphamic acid (SA) were optimized for the deposition of smooth Zn-Ni, Zn-Co and Zn-Ni-Co coatings on mild steel substrate. Bath compositions and deposition conditions were optimized by Hull cell method for maximum efficiency against depositions in corrosion. Faradic efficacy exceeded 90% as the current density increased; increased wt-% of nobler metal content (Ni and Co) in the deposit. Potentiodynamic polarization and electrochemical impedance spectroscopy indicates that the Zn-Ni-Co coating; corrosion resistance was 28 times higher than the Zn-Ni and 21 times higher than the Zn-Co coating. The good corrosion resistance of the Zn-Ni-Co coating was ascribed to its phase structure and the surface morphology. New cheap sulphate baths have been suggested for bright and uniform coating of Zn-Ni, Zn-Co and Zn-Ni-Co and result have been discussed.
Experimental study on electroforming of Ni-Co alloy with low internal stress
[J].
电铸低内应力Ni-Co合金实验研究
[J].
Electrochemical studies of zinc-nickel codeposition in sulphate bath
[J].
Study of the mechanical and structural properties of Zn-Ni-Co ternary alloy electroplating
[J].
Electrochemical deposition of zinc-nickel alloy coatings in a polyligand alkaline bath
[J].
Influence of bath concentration and pH on electrodeposition process of ternary Zn-Ni-Mo alloy coatings
[J].
Effect of ascorbic acid on stability of sulfate nickel-iron alloy electroplating bath
[J].
抗坏血酸对硫酸盐体系镍-铁合金镀液稳定性的影响
[J].
Effect of different complexing agents on Pb-Co thin-film electrodeposition
[J].
Estimation of stability constants of metal complexes
[J].
络合物稳定常数的计算
[J].
Electrochemical lithium storage performance of ternary Zn-Co-Ni alloy thin film as negative electrodes by electrodeposition method
[J].
Wear and corrosive behaviors of electroless Ni-LaCl3 composites on nanoporous ATO surface of Ti substrate
[J].
Internal stress in nickel-zinc alloys electrodeposited from sulphate solutions
[J].
Electrochemical polarization: I. A theoretical analysis of the shape of polarization curves
[J].
Structure and properties of composite Ni-Co-Mn coatings on metal interconnects by electrodeposition
[J].
LaCl3-modified Ni deposits on 3D-heterotypic porous Ti surface for strengthening its mechanical and electrochemical properties
[J].
Electrochemical deposition of γ-phase zinc-nickel alloys from alkaline aolution
[J].
Structural and corrosion protection properties of electrochemically deposited nano-sized Zn-Ni alloy coatings
[J].
Electrodeposition of nickel-zinc alloy coatings with high nickel content
[J].
Effect of electrodeposition conditions on the composition, microstructure, and corrosion resistance of Zn-Ni alloy coatings
[J].
Relationship of corrosion behavior between single-phase equiatomic CoCrNi, CoCrNiFe, CoCrNiFeMn alloys and their constituents in NaCl solution
[J].
Role of Ni content in improvement of corrosion resistance of Zn-Ni alloy in 3.5% NaCl solution. Part I: Polarization and impedance studies
[J].
Characterization of the influence of Ni content on the corrosion resistance of electrodeposited Zn-Ni alloy coatings
[J].