北京科技大学新材料技术研究院腐蚀与防护中心, 北京 100083
中图分类号: TG172.82
文献标识码: A
文章编号: 0412-1961(2016)06-0672-07
通讯作者:
收稿日期: 2015-11-4
网络出版日期: 2016-06-15
版权声明: 2016 《金属学报》编辑部 《金属学报》编辑部
基金资助:
作者简介:
作者简介: 许立宁, 男, 1976年生, 副教授, 博士
展开
摘要
利用高压釜, 研究了6.5%Cr钢在80 ℃和0.8 MPa CO2条件下的腐蚀行为. 利用SEM和EDS研究了腐蚀产物膜表面和截面微观形貌以及Cr在腐蚀产物膜中的富集状况. 利用高温高压电化学测试研究了线性极化电阻和电化学阻抗谱(EIS)随腐蚀时间的变化. 结合溶液离子浓度测试, 探讨了腐蚀产物膜生长机制. 结果表明, 6.5%Cr钢腐蚀速率为0.72 mm/a, 腐蚀产物膜中存在Cr的富集, Cr/Fe之比超过了5∶1. 不同腐蚀时间下, 溶液中Cr3+含量都很低, 说明Cr很少进入溶液.
关键词:
Abstract
In the oil and gas industry, CO2 in reservoirs generally causes severe corrosion of C steel in pipelines. Adding Cr to C steel can enhance CO2 corrosion performance by a factor of at least 3, and even up to 10 times and more, whilst maintain a cost penalty less than 1.5 times that of C steels. Corrosion behavior of 6.5%Cr steel in high temperature and high pressure CO2 environment is investigated in this work. The corrosion rate of 6.5%Cr steel at 80 ℃ and 0.8 MPa is measured by autoclave. The surface and cross-sectional morphology is studied by SEM, and the enrichment of Cr in the corrosion scale is investigated by EDS. The change of LPR and EIS results with corrosion time is studied by high temperature and high pressure electrochemical tests. According to the test results of ion concentration in the solution, the mechanism of corrosion scale growth is discussed. The results show that the corrosion rate of 6.5%Cr steel is 0.72 mm/a. The Cr enriches in the corrosion scale, and the Cr/Fe ratio is higher than 5∶1. Under different corrosion time, the concentration of Cr3+ in the solution is always low, which demonstrates that Cr seldom enters into solution.
Keywords:
在油气开采领域, 地层伴生的CO2气体会导致碳钢材质的油井管和集输管线发生严重腐蚀[1]. 我国各主要油气田含CO2区块较多, CO2腐蚀问题较为突出, 而加注缓蚀剂无法有效抑制局部腐蚀, 因此在苛刻CO2腐蚀环境下不能选用碳钢[2]. 人们把目标转移到耐蚀性能较好的不锈钢上, 但是不锈钢的成本较高、可焊性差, 且存在焊缝应力腐蚀开裂的风险[3]. 因此, 目前急需开发兼具低成本和高耐蚀, 并满足管线钢性能要求的低合金钢, 以填补碳钢和不锈钢之间的空白. 其中, 含Cr低合金钢由于耐蚀性能和机械性能良好, 最有潜力替代碳钢应用于CO2环境下[4], 已成为国内外研究热点.
在成分设计方面, Nice等[5]利用现场检测数据, 研究了Cr含量对油井管耐蚀性的影响, 发现提高Cr含量可显著延长服役寿命, 当Cr含量为0.5% (质量分数, 下同)时, 钢的腐蚀速率有所降低; 当Cr含量达到3%时, 腐蚀速率显著降低. 对于C和V等其它合金元素, Takabe和Ueda[6]发现, 当C含量从0.01%逐渐升高至0.18%时, 3%Cr钢的腐蚀速率从8.9 mm/a单调上升至11.1 mm/a. Kermani等[7]研究表明, 添加少量V元素, 可显著提高钢的耐蚀性.
围绕含Cr低合金钢的耐蚀机理, 多数学者[8,9]认为, 含Cr低合金钢的平均腐蚀速率低于碳钢的原因是, 其腐蚀产物膜的保护性高于碳钢. 例如, Muraki等[10]通过研究发现, Cr的活性比Fe高, 在活化状态下含Cr低合金钢的腐蚀速率比碳钢大, 但是形成腐蚀产物膜后, 含Cr低合金钢的腐蚀速率却显著降低, 因此, 耐蚀性能提高的关键因素是腐蚀产物膜. 一些学者认为, Cr会在腐蚀产物膜中富集, 显著改变了腐蚀产物膜的结构、致密度和稳定性, 从而提高耐蚀性能[11]. Takabe和Ueda[12]认为, 随着腐蚀产物膜中FeCO3的溶解, Cr会在膜中富集, 膜中Cr含量是基体中Cr含量的10倍以上. Ueda和Ikeda[13]认为Cr以非晶态Cr(OH)3的形式存在于腐蚀产物中, 使得钢基体溶解受到抑制.
在抗局部腐蚀性能方面, Chen等[14]研究了碳钢N80, 1Cr和4Cr钢的抗CO2局部腐蚀性能, 含Cr钢能够有效抑制点蚀, 当Cr含量达到4%时, 不发生点蚀. Kermani等[7]报道了当Cr含量为3%时可有效抑制台地腐蚀的发生, Cr元素的存在同时抑制碳钢的均匀腐蚀和局部腐蚀. Nice和Ueda [15]发现Cr元素的加入降低了局部腐蚀倾向, 而且降低腐蚀速率所需的最低Cr含量是温度的函数, 当Cr含量为1%~2%时, 在60 ℃时都发生了局部腐蚀, 加入Cu元素后, 不发生局部腐蚀.
在较高温度、较为苛刻的水质条件下, 需要更高的Cr含量才能保持较好的耐蚀性能, 而目前关于Cr含量>5%含Cr钢的研究非常少, 限制了含Cr钢的开发和应用. 本工作炼制了6.5%Cr钢, 并进行了控轧控冷, 利用高温高压釜研究了6.5%Cr钢的耐蚀性能, 采用扫描电镜(SEM)和能谱仪(EDS)对2个腐蚀周期下的腐蚀产物膜进行了研究, 同时借助电化学方法和溶液离子浓度测试, 对腐蚀初期的腐蚀过程进行了研究, 探讨了低Cr钢CO2腐蚀产物膜形成的机制, 为低Cr钢的研发提供重要参考.
实验材料为首都钢铁公司炼制的6.5%Cr钢, 其化学成分(质量分数, %)为: C 0.07, Cr 6.50, Mo 0.15, Si 0.20, Mn 0.55, Nb 0.03, Fe余量. 经控轧控冷工艺后, 材料的组织为贝氏体+铁素体, 如图1所示.
实验溶液为模拟某油田采出液, 采用化学纯99.9%试剂配置, 其离子含量(mg/L)为: Na+ 10300, Mg2+ 227, Ca2+ 990, K+ 337, SO42- 133, HCO3- 377, Cl- 18100, pH值为5.6. 腐蚀模拟实验在高温高压反应釜中进行, 腐蚀试样采用50 mm×10 mm×3 mm的挂片试样, 挂片一端开直径3 mm的圆孔, 利用钓鱼线悬挂于高压釜中, 如图2所示. 每组实验釜内装有5个平行样, 其中3个试样用于称量腐蚀前, 以及腐蚀后带膜、酸洗除膜后的质量, 用以计算试样的平均腐蚀速率, 其余2个试样分别用于表面及截面的微观形貌观察. 试样表面和截面形貌观察在JSE-6510A型SEM下进行, 采用JED-2300 EDS进行腐蚀产物的成分分析.
图2 进行失重法测试所用的高温高压反应釜示意图
Fig.2 Schematic of high temperature and high pressure (HTHP) autoclave used to perform weight loss test
实验前先在溶液中通入CO2除氧处理8 h, 然后将溶液装入高压釜中, 同时将试样放入溶液, 升温至实验温度80 ℃, 继续通入CO2除氧处理2 h后升压至0.8 MPa. 共进行2组高压釜实验, 实验周期分别为120和240 h. 高温高压电化学实验试样尺寸为10 mm×10 mm×3 mm, 试样底部用导线焊接后用环氧树脂密封, 测试表面用砂纸逐级打磨至800号, 依次用丙酮和酒精超声清洗后干燥. 线性极化电阻和电化学阻抗谱(EIS)使用PARSTAT4000电化学工作站在高温高压电化学测试反应釜中单独测试. 电化学测试采用三电极体系, 辅助电极为Pt电极, 参比电极为Ag/AgCl电极. 测量线性极化电阻时电位从-10 mV (vs Ecorr, Ecorr为开路电位)扫描至10 mV (vs Ecorr), 扫描速率为0.166 mV/s, EIS的测量频率范围为100 kHz~0.005 Hz, 振幅为5 mV. 电化学测试所采用的高温高压电化学釜如图3所示.
高压釜中溶液的离子含量的收集与测试步骤如下: 首先, 关闭进出气阀门, 卸下气瓶, 然后, 在进气管口接上10 mL的玻璃瓶, 缓缓打开进气管处的阀门, 利用釜内剩余压力, 将少量溶液挤入玻璃瓶. 收集完成后, 关闭进气管处的阀门, 恢复至收集溶液之前的状态. 所收集的溶液中的Fe2+和Cr3+离子的浓度使用Merck MOVA60A COD分析仪进行检测. 分别对腐蚀0, 2, 4, 6, 10, 12, 24, 48, 72, 96和120 h的溶液进行了检测.
图3 电化学测试所采用的高温高压电化学釜示意图
Fig.3 Schematic of HTHP autoclave used to perform electrochemical test (WE, CE and RE—working, counter and reference electrode)
6.5%Cr钢在80 ℃, 0.8 MPa CO2分压下的宏观腐蚀形貌如图4所示. 可见, 腐蚀240 h后, 表面形成一层很薄但致密、完整的膜(图4a), 酸洗除膜后, 表面平整, 没有出现局部腐蚀(图4b). 而碳钢X65在相同腐蚀环境下出现了严重的局部腐蚀[16].
图4 在80 ℃, 0.8 MPa分压下腐蚀240 h后6.5%Cr钢的宏观腐蚀形貌
Fig.4 Macroscopic morphologies of 6.5%Cr steel exposed under 80 ℃ and 0.8 MPa CO2 partial pressure for 240 h (a) before pickling (b) after pickling
实验周期为240 h时, 失重法得到的6.5%Cr钢腐蚀速率是0.72 mm/a, 而碳钢X65在相同腐蚀环境下(80 ℃, 0.8 MPa CO2分压, 静态)腐蚀517 h的腐蚀速率为9.83 mm/a, 3%Cr钢的腐蚀速率为1.37 mm/a[16]. 可见, 随着基体中Cr含量的增加, 低Cr钢腐蚀速率呈下降趋势, 但Cr含量超过3%之后, 下降趋势明显减缓. 实验周期为120 h时, 6.5%Cr钢的腐蚀速率为1.12 mm/a, 虽然实验周期为120 h和实验周期为240 h采用的不是同一个试样, 但是可以推测, 在120~240 h期间, 腐蚀产物膜的保护性略有提高, 因此腐蚀速率略有下降.
实验周期分别为120和240 h的腐蚀产物膜表面微观形貌如图5a和b所示. 对于低Cr钢, 由于腐蚀产物膜中出现Cr元素的富集, 而含Cr腐蚀产物从高压釜中取出后容易脱水开裂, 因此2个实验周期下的微观形貌都呈现龟裂状[17]. 此外, 在腐蚀产物膜表面还沉积了一些白色颗粒, 经EDS分析(图5c), 颗粒中不含Cr元素, 由Fe, O和C组成, 可知其为从溶液一侧沉积的FeCO3. 随着实验周期的延长, 白色颗粒有增多的趋势.
图5 6.5%Cr钢腐蚀产物膜表面微观形貌及白色颗粒的EDS分析
Fig.5 Corrosion scales microscopic morphologies of 6.5%Cr steel exposed for 120 h (a) and 240 h (b), and EDS analysis of white particle (c)
为了排除表面白色颗粒的干扰, 准确测定腐蚀产物膜中Cr富集程度, 制作了截面试样. 腐蚀120和240 h后, 截面形貌如图6a和b所示. 随着腐蚀时间的延长, 腐蚀产物膜厚度略有增加, 但与3%Cr钢相比(厚度约40 μm[18]), 腐蚀产物膜较薄. 采用EDS测定了腐蚀产物膜截面的成分, 如图6c和d所示. 可见, 腐蚀120 h时, 膜中的Cr/Fe的质量比约为1∶1, 而腐蚀240 h后, Cr/Fe之比超过了5∶1, 说明随腐蚀时间的延长Cr逐渐在腐蚀产物膜中富集. 从腐蚀产物膜微观形貌可知, 6.5%Cr钢比碳钢耐蚀的主要原因是生成了连续、致密的富Cr腐蚀产物膜, 这层膜的缺陷少、保护性较好. 表面沉积的白色颗粒(几乎不含Cr), 因为没有形成连续覆盖, 对基体起不到有效的保护作用. 因此, 下面重点探究这层富Cr膜的形成原因和生长机制.
图6 6.5%Cr钢腐蚀产物膜截面微观形貌及EDS结果
Fig.6 Cross-sectional microscopic morphologies (a, b) and corresponding EDS analyses (c, d) of 6.5%Cr steel scale exposed for 120 h (a, c) and 240 h (b, d)
对腐蚀120 h截面试样进行了面扫描分析, 如图7所示. 可见, Cr在腐蚀产物膜中是均匀分布的, 没有出现岛状聚集现象. 同样, 腐蚀240 h试样的腐蚀产物膜中, Cr也是均匀分布的. 假如富Cr膜的形成是由Cr3+从溶液一侧向试样表面沉积所造成的, 那么其分布形态应该像图5中的白色颗粒那样, 分布上应该存在一定程度的不均匀性.
图7 腐蚀120 h试样的截面SEM像及EDS面扫描结果
Fig.7 Cross-sectional SEM image of specimen exposed for 120 h (a), and EDS map scanning morphologies of Cr (b), Fe (c) and O (d)
120和240 h周期下的高压釜实验, 给出了连续、完整腐蚀产物膜形成之后6.5%Cr钢的腐蚀规律, 而腐蚀初期、腐蚀产物膜刚刚开始形成时, 腐蚀产物膜的生长过程很难通过高压釜实验来体现, 采用电化学手段可以实现连续监测, 能够弥补高压釜实验的不足. 图8给出了线性极化法得出的1/Rp (Rp为线性极化电阻, 利用1/Rp可以表征腐蚀速率)随时间(t)的变化规律. 可见, 在前24 h, 1/Rp快速下降, 之后缓慢下降, 在96 h以后, 基本达到稳定.
图8 线性极化法得出的1/Rp随时间(t)的变化规律
Fig.8 Linear polarization resistance (Rp) result of 1/Rp varying with time (t)
由于腐蚀产物膜生长过程中, 金属/溶液界面的电化学特性不断发生变化, 因而EIS可以用于探究腐蚀产物膜生长机制. 不同腐蚀时间下6.5%Cr钢的EIS如图9所示. 可见, 随着腐蚀时间的延长, 容抗弧逐渐增大, 说明腐蚀产物膜的保护性在不断提高. 10~48 h, 出现了明显的感抗弧; 72 h以后, 感抗弧消失, 呈现双容抗特性. 感抗的出现与阳极反应的中间产物FeOHad在钢表面的吸附有关, 双容抗的出现则表示试样表面已经形成了一层完整的腐蚀产物膜[19].
图9 不同腐蚀时间下6.5%Cr钢的Nyquist图
Fig.9 Nyquist diagram of 6.5%Cr steel exposed at different times
为了结合电化学数据体现的规律, 分析腐蚀产物膜生长过程, 进行了溶液中Fe2+和Cr3+含量的测试. 因为Fe和Cr发生腐蚀之后, 除了进入溶液之外, 就是形成了腐蚀产物膜, 测试溶液中的离子含量, 有利于分析Cr富集的过程. 该测试在高压釜中进行, 在不同腐蚀时间下, 将釜内的部分溶液导出, 由于取液管的尖端紧挨试样放置, 因而得到的是试样经高温高压CO2腐蚀后表面附近溶液的离子含量. 离子含量测试结果如表1所示, 溶液中Cr3+含量很低, 除了2, 6和96 h以外, 在其它实验周期下, Cr3+浓度都低于0.1 mg/L. 而Fe2+浓度在24 h出现峰值之后, 呈现上下波动, 24 h之前, 溶液中Fe2+浓度随腐蚀时间延长单调上升. 如图8所示, 1/Rp在4 h出现了明显的增大, 如图9所示, 在4 h时EIS容抗弧也出现了明显的减小, 这可能与Cr3+进入溶液导致酸化, 从而加速腐蚀有关. 因为表1所示, 在2~6 h期间, 溶液中Cr3+含量明显高于其他时段.
表1 高温高压CO2腐蚀后表面附近溶液的离子含量测试结果
Table 1 Ion concentration of the test solution near the 6.5%Cr steel surface after high temperature and high pressure CO2 corrosion under different times
| Time / h | Fe2+ / (mgL-1) | Cr3+ / (mgL-1) |
|---|---|---|
| 0 | 3.9 | <0.10 |
| 2 | 13.6 | 0.15 |
| 4 | 19.5 | <0.10 |
| 6 | 34.8 | 0.21 |
| 10 | 41.4 | <0.10 |
| 24 | 68.5 | <0.10 |
| 48 | 46.9 | <0.10 |
| 72 | 49.2 | <0.10 |
| 96 | 59.8 | 0.11 |
| 120 | 32.5 | <0.10 |
围绕Cr在腐蚀产物膜富集的过程, 国内外学者进行了较为深入的讨论, 建立了一些机理. 普遍认为低Cr钢在CO2腐蚀过程中, Cr优先腐蚀进入溶液, 以离子形式存在, 然后再逐渐沉积到钢表面, 形成含Cr腐蚀膜, 随着腐蚀时间的延长, 受某些因素的影响, Cr逐渐在腐蚀膜中富集, 最终形成了富Cr腐蚀产物膜[2,5,8,20]. 而根据6.5%Cr钢的上述实验结果可知, Cr是以直接成膜的方式, 在表面原位生长, 不需要经历腐蚀-进入溶液-逐渐沉积这一过程.
向钢中添加一定量的Cr后, 由于Cr原子的活性较高(Cr的电极电位明显低于Fe), 将优先发生活性溶解, 即当低Cr钢试样置于实验溶液中时, 固/液界面处的最外层Cr原子将优先发生活性溶解[21]:
(1) 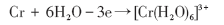
陈太辉[22]认为, Cr进入溶液后, 将发生水解和缩合反应, 附着在低Cr钢表面, 然后逐渐在腐蚀产物膜中富集:
(2) 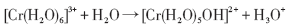
(3) 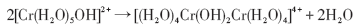
而Takabe和Ueda[6]认为, 随着腐蚀时间的延长, 腐蚀产物膜中的FeCO3会发生溶解, 留下的位置被含Cr化合物填充, 从而导致膜中Cr的富集.
本工作认为, 低Cr钢的腐蚀初期, Cr除了按照式(1)来腐蚀进入溶液以外, 在pH值适宜的环境下, 也会同时发生如式(4)的反应, 在失电子的同时直接在低Cr钢表面原位生成Cr(OH)3.
(4) 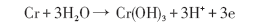
生成的Cr(OH)3附着在表面, 形成腐蚀产物膜. 溶液中的Fe离子也会向表面沉积, 形成FeCO3, 与Cr(OH)3一起组成腐蚀产物膜. 但由于FeCO3的沉积受临界过饱和度的控制, 低Cr钢表面附近常常呈现酸化特征[20], 酸化导致的pH值降低会大幅提高FeCO3的临界过饱和度, 因此FeCO3沉积量较少[23], 使得膜中Cr含量较高, 出现了膜中Cr元素含量高于基体的现象, 即Cr的富集. 随着腐蚀时间的延长, 腐蚀掉的Fe大部分都以离子形式进入了溶液, 腐蚀掉的Cr持续以Cr(OH)3的形式在腐蚀产物膜内累积, 从而导致膜中Cr含量进一步升高, 最终呈现膜中Cr高度富集的状况. 当试样从高压釜中取出后, Cr(OH)3很容易脱水生成Cr2O3, 如式(5)所示, 导致腐蚀膜出现龟裂.
(5) 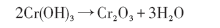
假如Cr的富集是通过溶解膜中已有FeCO3来实现的, 那么图6所示的2种实验周期下的Cr/Fe之比就很难解释了. 120 h腐蚀产物膜中的Cr/Fe之比为1∶1, 腐蚀240 h就显著增大为5∶1, 假如是FeCO3溶解机制控制的, 那么需要把腐蚀膜中已经存在的大部分FeCO3都溶解掉, 才能实现5∶1的Cr/Fe比, 这显然是很难实现的.
假如Cr必须经历腐蚀-进入溶液-逐渐沉积才能在膜中富集, 那么在腐蚀初期, 溶液中Cr3+浓度应该较高, 但是表1显示, Cr3+含量很低, 通常测不出来. 对比不同腐蚀时间下溶液中Fe2+和Cr3+浓度的变化规律也可以证明, Cr没有大量进入溶液. 普遍认为, Fe是要经历腐蚀-进入溶液-逐渐沉积这一过程的, 因而表1中前24 h, Fe2+浓度单调上升, 说明此阶段, Fe在逐渐进入溶液. 随着腐蚀产物膜保护性的提高, Fe腐蚀的速率在24 h以后明显低于24 h以前(图8), 进入溶液的Fe2+会减少, 此外, 随着FeCO3在表面的沉积, 溶液中Fe2+也会减少, 因而导致在24 h出现了Fe2+浓度的峰值. 对比Fe2+和Cr3+浓度的变化可以看出, Cr没有像Fe那样逐渐进入溶液, 如果没有进入溶液, 就极有可能在腐蚀产物膜中逐渐富集.
Zhu等[24]发现, 3Cr钢在测试阳极极化曲线的过程中, 表面会生成一层Cr(OH)3膜. 因为极化曲线测试时间很短, 且Cr(OH)3沉积需要一定时间和满足一定的过饱和条件, 所以认为这层Cr(OH)3膜是原位生成的. 这也从侧面说明, 表面生成Cr(OH)3膜不需要Cr先进入溶液.
6.5%Cr钢在80 ℃, 0.8 MPa条件下腐蚀240 h, 腐蚀速率是0.72 mm/a. 6.5%Cr钢腐蚀120 h, 腐蚀产物膜中的Cr/Fe之比约为1∶1, 腐蚀240 h, Cr/Fe之比超过了5∶1. 不同腐蚀时间下, 溶液中Cr3+含量都很低, 而Fe2+浓度在24 h出现峰值之后, 呈现上下波动, 24 h之前, 溶液中Fe2+浓度随腐蚀时间延长单调上升.
The authors have declared that no competing interests exist.

/
| 〈 |
|
〉 |